Bienestar y deporte
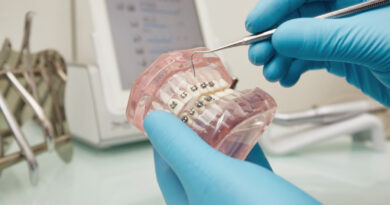
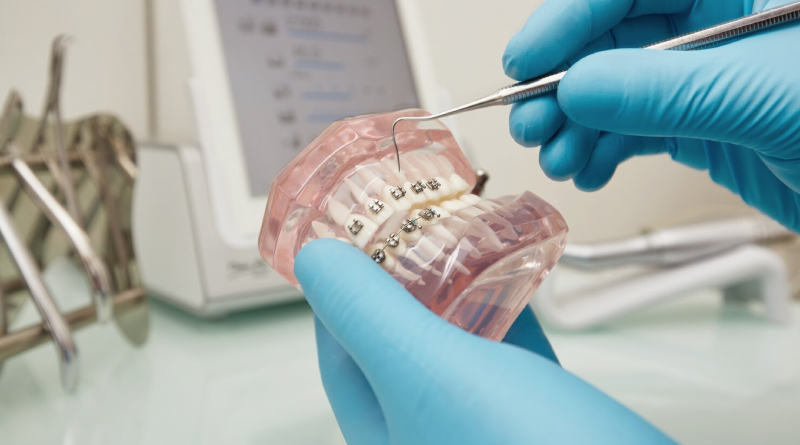
Los mitos más comunes sobre la ortodoncia, ¡derribados!
Muchos pacientes pasan toda su vida creyendo en muchos de los mitos más comunes sobre la ortodoncia. Pueden pensar que
Tecnología

El avance de la tecnología: La realidad virtual y la IA redefine las apuestas deportivas
El mundo de las apuestas deportivas ha experimentado cambios revolucionarios en las últimas décadas. Desde los primeros pronósticos en papel
Empresa y Economía

Lo que debes saber antes de invertir en Bitcoin
Las criptomonedas se han convertido para muchos en uno de los activos de inversión de alto riesgo más interesantes de
Viajar

Esquiar en Andorra: guía esencial para aprovechar al máximo sus pistas
¿Planificando tus vacaciones invernales? Andorra es una de las alternativas predilectas a la hora de organizar una escapada llena de
Sexualidad

Explorando las Dinámicas de Poder en las Relaciones Modernas
En las últimas décadas, hemos sido testigos de una evolución significativa en las dinámicas de poder dentro de las relaciones